中国科学院分子细胞科学卓越创新中心许琛琦研究组与上海科技大学王皞鹏研究组合作,通过蛋白设计,构建了可相分离的新型E-利来国际ag旗舰厅CAR分子,提高了免疫突触质量,从而提高了抗原敏感性和细胞持续性,在动物模型中取得良好疗效。日前,相关成果在线发表于《免疫》。
传统二代嵌合性抗原受体(CAR)是一种人工合成的免疫受体。利用基因工程方法在T细胞中外源表达CAR后,产生的CAR T细胞可以针对特定抗原产生免疫应答反应,可用于治疗肿瘤、自身免疫病、感染、器官纤维化等多种疾病。
然而,与天然的T细胞抗原受体(TCR)相比,CAR的抗原敏感性差,与其它信号分子的协同性差。CAR无法像TCR一样形成成熟的免疫突触来整合各条信号通路。优化CAR的信号转导功能是突破当前CAR T细胞治疗临床瓶颈的关键所在。
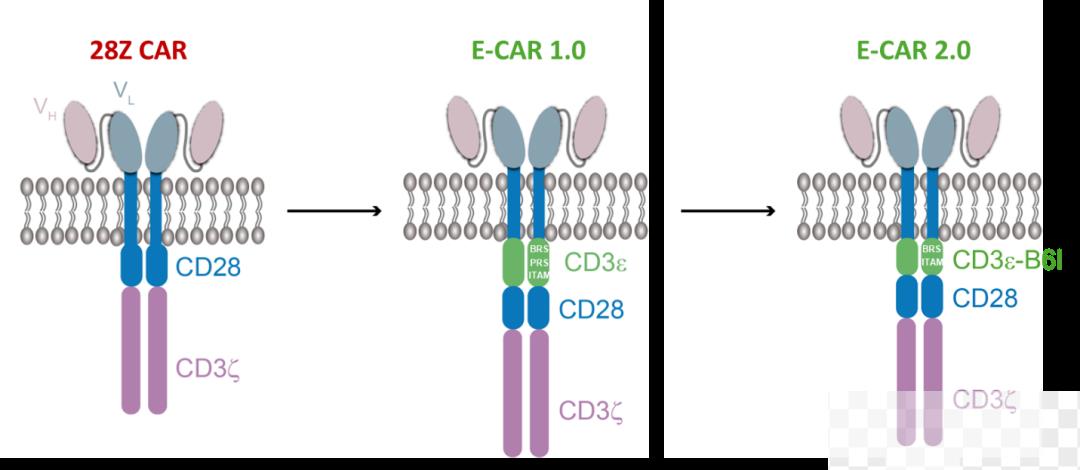
团队将CD3ε引入二代CAR分子,设计出了在功能上更加模拟TCR的第一代E-CAR。团队发现E-CAR 1.0的胞内信号区自身就能够形成液液相分离,而传统二代CAR分子的相分离现象较弱,因此通过蛋白序列优化,构建了一种E-CAR 2.0版本,在保留其相分离所需碱性氨基酸的基础上,有效地提高了膜表达水平。
?
由于抗原受体聚集是免疫突触形成的基础,E-CAR相分离促进了免疫突触成熟,不仅提升了E-CAR在中央超分子激活簇(cSMAC)中的信号转导功能,还在外周形成更好的CD2花冠结构,招募PI3K这些信号分子来介导共刺激信号。团队还注意到,E-CAR免疫突触呈现出信号先放大后减弱的动态性,与TCR形成的免疫突触非常相似。
随后,团队对E-CAR T细胞的功能展开了研究,发现其对弱抗原肿瘤细胞的结合与杀伤都更强。通过建立肿瘤细胞反复刺激模型,团队发现E-CAR T细胞的长效杀伤效果更好,在清除肿瘤细胞的同时还可维持自我增殖。RNA测序结果显示E-CAR T细胞可以利用CD2信号来缓解功能耗竭,这与其能诱导形成CD2花冠结构这一现象吻合。在血液瘤和实体瘤的初发肿瘤动物模型以及血液瘤复发的动物模型中,E-CAR T细胞都比传统的细胞表现出了更好的抗肿瘤效果。
相关论文信息:
https://doi.org/10.1016/j.immuni.2024.11.005
